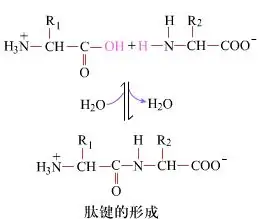
Səthdə dipeptidlər verən peptid bağlarının əmələ gəlməsi sadə kimyəvi prosesdir.Bu o deməkdir ki, iki amin turşusu komponenti susuzlaşdırılarkən peptid bağı, amid bağı ilə bağlıdır.
Peptid bağının formalaşması mülayim reaksiya şəraitində bir amin turşusunun aktivləşməsidir.(A) karboksil hissəsi, ikinci amin turşusu (B) Nukleofil aktivləşdirilmiş karboksil hissəsi daha sonra dipeptidi (AB) əmələ gətirir."Əgər karboksil komponenti (A) qorunmursa, peptid bağının meydana gəlməsinə nəzarət edilə bilməz."Xətti və siklik peptidlər kimi əlavə məhsullar hədəf birləşmələri AB ilə qarışdırıla bilər.Buna görə də, peptid bağının formalaşmasında iştirak etməyən bütün funksional qruplar peptid sintezi zamanı müvəqqəti geri çevrilən şəkildə qorunmalıdır.
Beləliklə, peptid sintezi - hər bir peptid bağının formalaşması - aqreqasiyanın üç mərhələsini əhatə edir.
İlk addım qorunmağa ehtiyacı olan bəzi amin turşularını hazırlamaqdır və amin turşularının zvitterion quruluşu artıq mövcud deyil.
İkinci addım, peptid bağlarının meydana gəlməsi üçün iki mərhələli reaksiyadır, burada N-mühafizə olunan amin turşusunun karboksil qrupu əvvəlcə aktiv ara məhsula qədər aktivləşir və sonra peptid bağı əmələ gəlir.Bu birləşmiş reaksiya bir addımlı reaksiya və ya iki ardıcıl reaksiya şəklində baş verə bilər.
Üçüncü addım qoruyucu bazanın seçmə çıxarılması və ya tamamilə çıxarılmasıdır.Bütün çıxarılması yalnız bütün peptid zəncirləri yığıldıqdan sonra baş verə bilsə də, peptid sintezini davam etdirmək üçün qoruyucu qrupların selektiv çıxarılması da tələb olunur.
Çünki 10 amin turşusu (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec və Cys) yan zəncirli funksional qrupları ehtiva edir ki, bu da selektiv qorunma tələb edir, bu da peptid sintezini çətinləşdirir.Müvəqqəti və yarı daimi mühafizə əsasları seçiciliyə dair müxtəlif tələblərə görə fərqləndirilməlidir.Amin turşusu və ya karboksil funksional qruplarının müvəqqəti qorunmasını əks etdirmək üçün növbəti mərhələdə müvəqqəti qoruma qrupları istifadə olunur.Yarı daimi qoruyucu qruplar, bəzən sintez zamanı artıq formalaşmış peptid bağlarına və ya amin turşusu yan zəncirlərinə müdaxilə etmədən çıxarılır.
"İdeal olaraq, karboksil komponentinin aktivləşdirilməsi və peptid bağlarının sonrakı formalaşması (birləşmə reaksiyaları) rasemik və ya əlavə məhsul meydana gəlmədən sürətli olmalıdır və yüksək məhsul əldə etmək üçün molar reaktivlər tətbiq edilməlidir."Təəssüf ki, kimyəvi birləşmə üsullarının heç biri bu tələblərə cavab vermir və bir neçəsi praktiki sintez üçün uyğundur.
Peptid sintezi zamanı müxtəlif reaksiyalarda iştirak edən funksional qruplar adətən əl mərkəzi ilə əlaqələndirilir, qlisin yeganə istisnadır və potensial fırlanma riski var.
Peptid sintezi dövrünün son mərhələsi bütün qoruyucu qrupların çıxarılmasıdır.Qoruyucu qrupların selektiv çıxarılması, dipeptid sintezində mühafizənin tam aradan qaldırılması tələbinə əlavə olaraq peptid zəncirinin uzadılması üçün vacibdir.Sintetik strategiyalar diqqətlə planlaşdırılmalıdır.Strateji seçimdən asılı olaraq, N α-amino və ya karboksil qoruyucu qrupları seçici şəkildə çıxara bilər.“Strategiya” termini ayrı-ayrı amin turşularının kondensasiya reaksiyalarının ardıcıllığına aiddir.Ümumiyyətlə, tədricən sintez və fraqment kondensasiyası arasında fərq var.Peptid sintezi (“ənənəvi sintez” kimi də tanınır) məhlulda baş verir.Əksər hallarda peptid zəncirinin tədricən uzanması yalnız qısa fraqmentləri sintez etmək üçün peptid zəncirindən istifadə etməklə sintez edilə bilər.Daha uzun peptidləri sintez etmək üçün hədəf molekulları müvafiq fraqmentlərə bölmək və onların C terminalında differensiasiya dərəcəsini minimuma endirə biləcəyini müəyyən etmək lazımdır.Fərdi fraqmentlər tədricən yığıldıqdan sonra hədəf birləşmə birləşdiriləcəkdir.Peptid sintezinin strategiyası ən yaxşı və ən uyğun qoruyucu fraqmentin seçilməsini, peptid sintezinin strategiyasına isə qoruyucu əsasların ən uyğun kombinasiyasının və fraqmentlərin birləşməsinin ən yaxşı metodunun seçilməsini əhatə edir.
Göndərmə vaxtı: 19 iyul 2023-cü il